Photochemisch orthogonale Festphasensynthesen
Kurzinformation
inkl. MwSt. Versandinformationen
Artikel zZt. nicht lieferbar
Artikel zZt. nicht lieferbar

Beschreibung
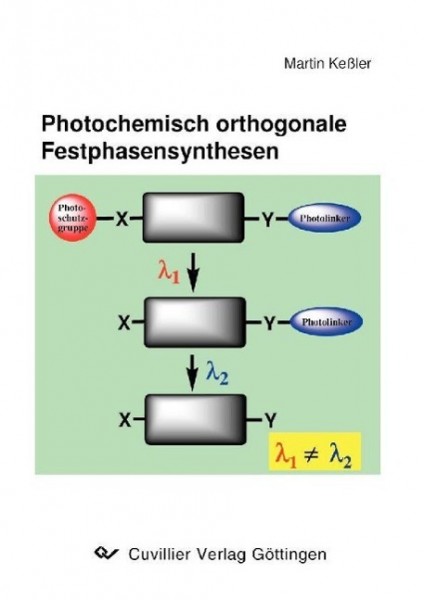
Schutzgruppenstrategien, in denen Licht als Abspaltungsreagens eingesetzt werden kann, sind eine interessante Erweiterung des chemischen Methodenarsenals, da unter milden, substratschonenden Bedingungen und ohne Kontamination der Substrate mit Reagentien gearbeitet werden kann.Es wurde eine photochemisch orthogonale Schutzgruppenstrategie für die Festphasen-Peptidsynthese entwickelt. Die Kombination von Pivaloyllinkern- und NVOC-Schutzgruppen wurde zu diesem Zweck eingehend untersucht. Die photochemisch orthogonale Methode erlaubte die wellenlängenselektive Anregung verschiedener photolabiler Schutzgruppen und lieferte die Zielverbindungen ohne weitere Aufarbeitung in hoher Reinheit.Die Brauchbarkeit des photolabilen Pivaloyllinkers zur Synthese größerer caged-Peptide (7 - 15 Aminosäuren) nach konventionellen Peptidsyntheseprotokollen und anschließender photolytischer Freisetzung (uncaging) der C-terminal gebundenen Peptide unter in-vivo-Bedingungen wurde untersucht.Schutzgruppenstrategien, in denen Licht als Abspaltungsreagens eingesetzt werden kann, sind eine interessante Erweiterung des chemischen Methodenarsenals, da unter milden, substratschonenden Bedingungen und ohne Kontamination der Substrate mit Reagentien gearbeitet werden kann.Es wurde eine photochemisch orthogonale Schutzgruppenstrategie für die Festphasen-Peptidsynthese entwickelt. Die Kombination von Pivaloyllinkern- und NVOC-Schutzgruppen wurde zu diesem Zweck eingehend untersucht. Die photochemisch orthogonale Methode erlaubte die wellenlängenselektive Anregung verschiedener photolabiler Schutzgruppen und lieferte die Zielverbindungen ohne weitere Aufarbeitung in hoher Reinheit.Die Brauchbarkeit des photolabilen Pivaloyllinkers zur Synthese größerer caged-Peptide (7 - 15 Aminosäuren) nach konventionellen Peptidsyntheseprotokollen und anschließender photolytischer Freisetzung (uncaging) der C-terminal gebundenen Peptide unter in-vivo-Bedingungen wurde untersucht.
Produktdetails

So garantieren wir Dir zu jeder Zeit Premiumqualität.
Über den Autor

- hardcover
- 279 Seiten
- Erschienen 1993
- Springer

- Gebunden
- 267 Seiten
- Erschienen 2013
- Springer

- Gebunden
- 421 Seiten
- Erschienen 2021
- Wiley-VCH

- Gebunden
- 696 Seiten
- Erschienen 2001
- Wiley-VCH

- hardcover
- 304 Seiten
- Erschienen 1999
- Springer

- Gebunden
- 324 Seiten
- Erschienen 2013
- Springer

- Gebunden
- 159 Seiten
- Erschienen 2012
- Springer

- Gebunden
- 292 Seiten
- Erschienen 2013
- Springer

- spiral_bound
- 272 Seiten
- Erschienen 2011
- Wiley

- Gebunden
- 392 Seiten
- Erschienen 2014
- Springer

- Hardcover -
- Erschienen 1978
- Harri Deutsch

- hardcover
- 484 Seiten
- Erschienen 2011
- Taylor & Francis Ltd

- Kartoniert
- 352 Seiten
- Erschienen 2003
- W.V.

- paperback
- 116 Seiten
- Erschienen 1937
- Springer